美两大制药暂停新冠疫苗临床实验 中俄大规模预约接种风险知多少?(组图)
上个星期,美国强生制药和礼来制药研发中的新冠疫苗和新冠抗体药物,因为有志愿者出现不良反应,喊停临床实验,再次提醒各国开发新冠药物过程中的风险,以及透明度和安全保障机制的重要性。
可是在另一方面,中国和俄罗斯大规模开放预约接种新冠疫苗。
那么,美国两大制药公司的挫折会不会提高新冠疫苗审批的门槛,和推迟疫苗诞生的时间?中俄广泛接种实验中的新冠疫苗会带来哪些风险?北京加入新冠疫苗保障机制后,中国疫苗是否被广泛接受?

志愿者出现不良症状 美国暂停新冠疫苗实验
由于试验参与者出现了不明原因的疾病,这方面的其中两项试验在美国已经暂停,分别是牛津大学和阿斯利康的一项试验以及强生公司的一项试验。
据美国之音报道,美国新冠疫苗研发领先者强生,因为一名参加实验的志愿者出现原因不明的不良症状,10月12日宣布暂停实验。强生对外发表的公告说,出于保护志愿者的隐私,不便透露具体情况。强生三期临床实验是新冠疫苗开发中规模最大的实验,有6万名志愿者参加。原沃尔特·里德陆军研究所病毒专家林晓旭博士说,在大型实验中有人出现不良反应是常见的。
他说:“通常对于疫苗的临床试验,特别是到第三期的临床试验,因为参与的志愿者相当多,比如强生的试验就有6万多人的注册,这个量是非常大的,所以当然遇到不良反应,特别是严重的不良反应,就是severe adverse这样的案例应该断断续续都会出现,这才是三期临床试验特别要注意的一点。”
林晓旭说,因为安全性只有在足够大人群里测试过以后,才会发现难以预测的情况,特别是一些系统性的不良反应。
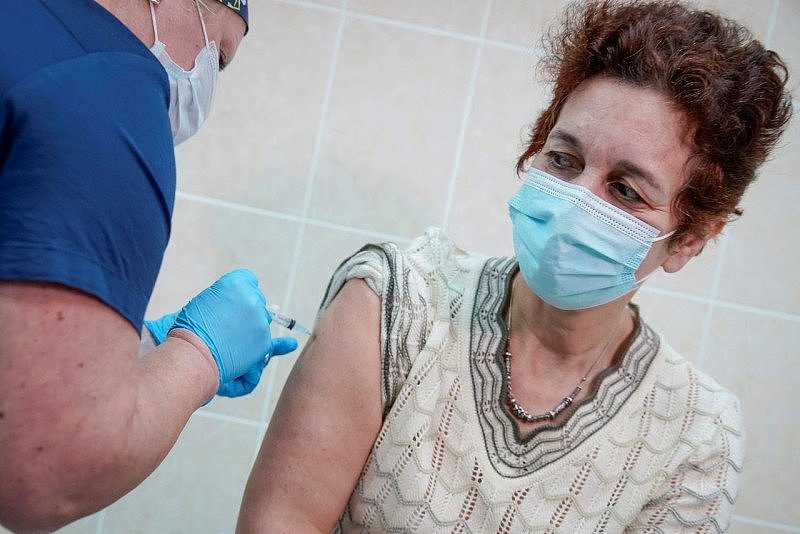
星期二,美国药厂礼来也因潜在安全疑虑,中止新冠抗体药物最后阶段的临床试验。9月初,英国制药商阿斯利康的新冠疫苗临床实验也因为有志愿者出现不良反应,喊停全球的实验。有人担心,这些挫折是否会提高疫苗审批的门槛,推迟疫苗诞生的时间。
林晓旭说,疫苗和药物的审批标准在开始试验前就已经制定,不会修改。不过,在疫苗开发中受到挫折,接下来将由第三方独立监督机构独立数据安全监控委员会和内部的临床和安全医生进行审查,可能会需要更长时间来做试验,影响疫苗的推出时间。
中俄大规模预约接种疫苗引发质疑
美国和欧洲还在等待新冠疫苗大规模临床试验结果然后再进行部署之际,中俄早已经开始大规模对实验性候选疫苗投入紧急使用,以期阻止全球感染人数上升的趋势。
据《南华早报》报道,中国国药集团这个还没有完成三期实验的新冠疫苗,已经在北京和武汉开放预约接种,并且给即将出国的留学生优先免费注射,报名者2个星期后可以到指定地点接种。
到10月13号星期二为止,已经有15万5千多人报名,76万多人表示有兴趣。
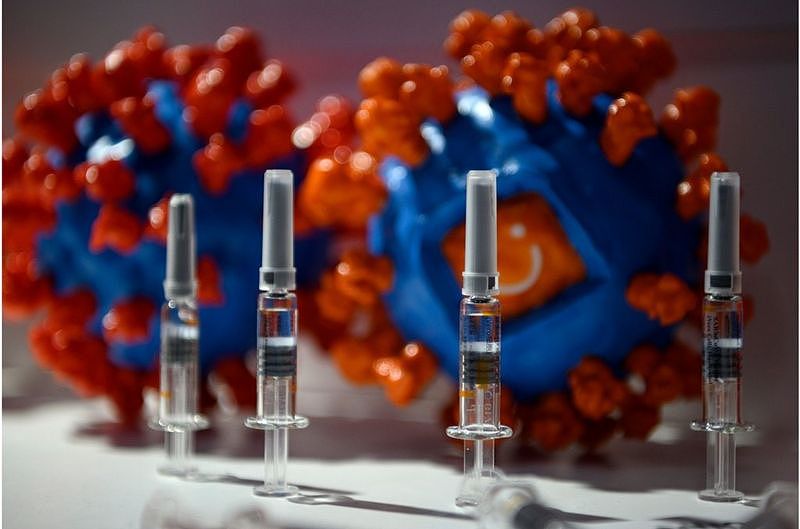
此外,中国嘉兴市疾病预防控制中心15日表示,该市启动新冠疫苗接种 ,疫苗由中国民营企业科兴生物技术公司研发,目前在嘉兴市被用于“紧急使用”。该机构称,政府会优先考虑从事相对高风险工作的人群,包括医疗人员、港口检查员和公共服务人员。
据了解,自今年7月以来,中国疫苗生产商已经为数万名国企员工、政府官员和疫苗公司高管接种了疫苗。中国政府最近几周表示,将把这项活动面向的人群扩大到教师、游客和超市员工。
16日,浙江省负责疫情防控工作的高级官员陈广胜表示,嘉兴所在的东部省份浙江省已“稳妥有序推进秋冬季新冠疫苗紧急接种”。他补充说,浙江也已经开始“重点推荐对象自愿接种工作”。
陈广胜在新闻发布会上说,政府已经注射了74.3万剂流感和冠状病毒疫苗。一位官员拒绝提供详细情况。
此外,据华尔街日报报道,过去一个月,阿联酋已经在向数千名医务工作者、教师、机场工作人员和政府官员提供一款中国疫苗,这是在中国以外规模最大的紧急使用计划。印尼一名高级卫生官员表示,印尼计划最早在下个月启动类似的紧急接种计划,涉及三种中国新冠疫苗。
俄罗斯在8月份批准为前线人员接种俄产新冠疫苗Sputnik V之后,近日也批准了第二种疫苗的紧急使用,俄罗斯总统普京表示,将加大这两种疫苗的生产。
专家表示:中俄做法是一个危险的押注
对于中国国药集团这种扎堆预约接种疫苗的现象,林晓旭说,这是非常不合理的,因为就算是非常成功的疫苗,在这样大疫情之下,也应该考虑哪些地区的疫情比较严重,哪些医疗机构人员更需要打疫苗,而不是让民众来哄抢。
他指出,国药公司这么做实际上是为了配合他们公司的股票升值的问题,是一种炒作。
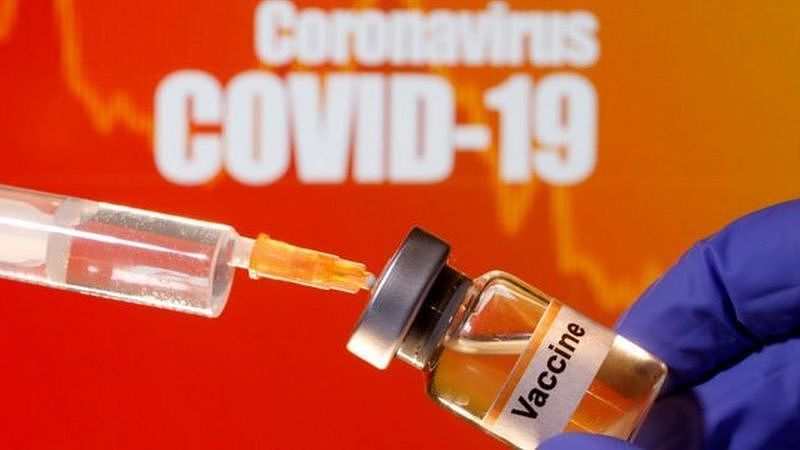
随后又有报道说,国药集团的官网上撤掉了报名的通道。有关这个消息,国药并没有出面澄清这个消息。这种缺乏透明度的做法令人质疑。
西方一些卫生专家警告说,疫苗的副作用和有效性还未确定,俄罗斯和中国的行动过快。这两个国家都在尝试利用疫苗外交及其他举措提升全球影响力,对抗美国及其盟友。特别是中国,中国将其在抗击疫情方面的成功作为其威权制度优于西方民主制度的证明。
位于伦敦的国际战略研究所欧洲问题高级顾问François Heisbourg称:“没什么能保证这些疫苗的有效性,也没什么能保证接种这些疫苗的人的安全。这是一个危险的押注,俄罗斯和中国的做法可能适得其反。”Heisbourg还称:“但实际结果如何只有做了才知道:如果成功了,他们会显得非常聪明,非常有先见之明,并会宣布他们有更好的模式。”
都柏林圣三一大学教授、免疫学家Luke O'Neill称:“我们必须极为严谨地对待疫苗开发。”O'Neill表示:“风险在于,如果疫苗存在安全问题,将会威胁到任何疾病的疫苗接种。”
对新冠疫苗保障机制的不信任
10月8日,中国中国宣布正式加入“新冠肺炎疫苗实施计划”。中方称这是推动疫苗成为全球公共产品的一个重要举措。
中国此前一直未明确表态是否加入,中国专家解读为做法“谨慎”,因其想平衡中国国内需求和邻国等需求。
不过,中国产的疫苗并非在每个区域都受欢迎,比如台湾福卫部长陈时中明确表示,台湾将不买中国疫苗。
世卫组织执委会成员,欧盟首席疫苗谈判代表克莱门斯·奥尔也表示,这个机制的透明度严重不足。他说:“我们对于疫苗的价格、质量、技术平台或风险都将没有发言权,这是完全无法接受的。”
林晓旭说:“如果中国的疫苗现在跳过了3期临床实验,带来很多国家对他质量的质疑,包括俄罗斯也是面临这样一个处境,对不对?如果这些疫苗的质量没法保住,我为什么非得加入这个机制,在一种不透明情况下去预定这些疫苗呢?所以我觉得最核心的问题仍然是疫苗是不是安全,是否有效,这是所有国家最先考虑的。”
他说,在购买渠道上,每个国家都会想自己的办法,不一定需要联合国在其中协调。
新冠疫苗何时能放心打?三期临床试验有多重要?
10月16日,江苏省疾病预防控制中心副主任朱凤才接受《科技日报》专访表示,对于新冠疫苗来说三期临床至关重要,因为它的任务就是用严谨、详实的科学数据证明疫苗是不是安全、有效。

三期临床试验主要是评价疫苗的保护效力。它的“三昧真火”是用真正的流行发病区域、大样本量(成千上万)、2个流行季来考验疫苗。
为保障持久的考验,三期临床试验的验证时间相对而言是刚性的,一般来说需要2-5年时间,对于传染病来说,需要经过至少两个流行季。
经过“三昧真火”的检验,很多备选疫苗会败下阵来:艾滋病疫苗人体临床试验已失败200余次,还有一些呼吸道传染疾病的疫苗也尚未成功。
“新冠疫苗的三期临床由于疫情防控的紧迫性,目前认为受试者全程免疫后需要持续至少2个月时间,而现在流行的12月底见分晓的说法主要是指获得初步结果(如做到一半的数据)的时间。”朱凤才说,只有这样,疫苗本身、疫苗与人体间的相互作用、临床研究方法的选择等这些可能出现纰漏的地方,才有可能被发现,进而不断地修正,以避免在上市大量使用时出现事故。
残酷的验证,三期临床试验有效的前提是“有人感染”!
疫苗的保护效力是多少?这也只有三期临床能给出的答案。
还有一些需要长期观察才会获得解答的问题。例如,疫苗急性毒性反应是怎样的,疫苗的免疫病理反应如何?
朱凤才说,只有严重不良反应、疫苗相关的特定的不良反应、接种疫苗后仍发生了重症病例等,会左右疫苗的命运。
而疫苗的免疫病理反应则需要接种较多的人群并随访观察更长时间才会显现出来,因为机体的免疫反应是体内一个十分复杂的过程。
专题:世界各国应对新冠肺炎疫情进入专题 >>
科学家发现可彻底改变新冠治疗方法的蝙蝠基因(图)
外媒:密苏里因新冠告中国!要求赔偿损失并威胁没收资产(图)
《华尔街日报》:特朗普拟叫停被指引发新冠疫情的病毒研究(组图)









 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


